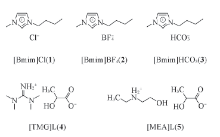
离子液体和醇胺溶液复配脱硫剂吸收H2S及再生性能
H2S是一种有刺激性气味的剧毒气体, 主要来源于天然气开发、 煤气化、 石油炼制、 合成氨工业、 污水处理以及造纸等生产过程, 对人类和环境造成极大危害. 同时, 在工业生产和运输过程中, 也会造成催化剂中毒和管路的严重腐蚀[1~3]. 随着工业发展和环保要求的提高, H2S的含量受到日益严格的限制. 因此研究一种高效吸收、 脱除H2S的方法具有十分重要的理论和现实意义. N-甲基二乙醇胺(MDEA)水溶液吸收H2S的方法由于其显著的节能效果, 并具有脱硫效率高、 腐蚀轻、 胺液不易降解等优点而成为气体脱硫的主体工艺之一[4~7], 但MDEA溶液存在容易发泡的缺点, 这会导致系统处理能力下降、 溶液再生不合格、 雾沫夹带严重使溶液损耗增加及净化气质量不达标等一系列问题, 严重影响装置的正常运行. 添加适宜的复配组分, 特别是有增进吸收和消减泡沫双重功效的复配剂, 是亟待开发的有效措施之一.
近年来, 在酸性气体的液相吸收领域, 人们在开发新的醇胺水溶液脱硫剂[8~10]的同时, 还对离子液体进行了应用探索. 离子液体(IL)作为环境友好型溶剂, 在吸收H2S等酸性气体方面引起了广泛关注[11~14]. 它具有一般脱硫剂无法比拟的优势: 蒸气压极小, 避免了吸收剂因挥发而造成的损失和污染; 功能化离子液体对酸性气体中的含硫组分具有优异的吸收能力; 其吸收性能可通过选择适宜的阴阳离子及其取代基而进行设计和调变, 从而满足实际需要[15~20]. Guo等[21]研究了己内酰胺四丁基溴化铵离子液体对H2S的吸收与空气氧化, 结果表明H2S在这种功能化离子液体中具有较高的溶解度, 并且溶解度随着己内酰胺比例的增加而增大, 随着温度的升高而急剧降低. Heintz等[22]制备了离子液体混合物TEGO IL K5(椰油烷基二羟乙基甲基氯化季铵盐乙氧基化物), 并研究了其对H2S和CO2的吸收性能, 结果表明, 较高的H2S溶解性能使得该离子液体更适于对H2S的捕集.
Duan等[23]考察了SO2在己内酰胺四丁基溴化铵离子液体水溶液体系中的溶解度, 发现SO2在该体系中的吸收与解吸是可逆的, 同时也确定了SO2是使离子液体与水两相分离的关键物质. 目前, 有关离子液体与醇胺水溶液复配吸收酸性气体的研究报道相对较少, 但由于混合体系不仅能够汇集单一体系的各自优势, 还有望克服其现有的缺点(如离子液体价格昂贵且对气体的分散性差而醇胺溶液则容易发泡), 因而具有很大的研发潜力. 目前, 已经开展了关于离子液体与醇胺水溶液混合体系黏度等性质的研究[24], 以及类似混合组分对CO2的吸收性能评价[25], 但在复配体系吸收H2S的实验或理论工作尚未见报道.
本文基于醇胺溶液与离子液体兼容体系优势互补的理念, 在有效消减醇胺发泡及大幅度降低离子液体用量的原则下, 考察了5种离子液体([Bmim]HCO3, [TMG]L, [MEA]L, [Bmim]Cl和[Bmim]BF4)与MDEA水溶液复配脱硫剂在不同条件下对H2S的吸收性能、 离子液体的消泡能力以及脱硫剂的再生性能, 并将实验研究与密度泛函理论计算相结合, 分析了复配体系的脱硫机理, 为后续的应用开发奠定了理论基础.
1 实验部分
1.1 试剂与仪器
N-甲基二乙醇胺(MDEA, 纯度为99%, 上海国药集团化学试剂有限公司); 1-丁基-3-甲基咪唑四氟硼酸盐([Bmim]BF4)、 氯化1-丁基-3-甲基咪唑([Bmim]Cl)、 1-丁基-3-甲基咪唑碳酸氢盐([Bmim]HCO3)、 乙醇胺乳酸盐([MEA]L)和1, 1, 3, 3-四甲基胍乳酸盐([TMG]L)纯度均为99%(上海成捷离子液体有限公司). 高纯硫化氢(纯度99.99%)、 高纯氮气(纯度99.999%)和高纯氧气(纯度99.999%)(济南德洋特种气体有限公司). 电化学测试用水为高纯水, 其它实验用水均为去离子水.
采用北京七星华创电子有限公司的D08-1D/ZM型(N2)和D08-1F型(H2S)质量流量计控制各气体流量; 采用武汉天虹仪器仪表集团的TH-990S型H2S分析仪检测气体浓度; 温度采用河南予华仪器有限公司的DF-101S集热式恒温加热磁力搅拌器控制, 无级调速0~2600 r/min; 采用美国TA公司SDT Q600型DSC/TGA同步热分析仪测定脱硫剂的热稳定性; 采用美国Thermo Nicolet 公司Avatar370型傅里叶变换红外光谱仪表征合成的离子液体; 采用济南瑞清臭氧设备有限公司提供的RQ系列臭氧发生器将高纯氧转化成臭氧对空气再生后的脱硫剂进行深度氧化; 采用戴安DX-120型离子色谱仪对臭氧深度处理的再生液进行离子检测及浓度分析, 由于长时间的吸收及再生过程, 不可避免地产生水分蒸发, 使吸收剂的质量和体积均有一定程度的减少, 考虑到从吸收器中转移溶液的过程中会造成溶质损失, 因此使用去离子水将吸收器洗涤3次定容至100 mL后进行测试.
1.2 实验过程
将离子液体、 MDEA和水按一定比例混合得到复配脱硫剂, 脱硫剂每次用量为10 mL, H2S气体流量为100 mL/min, 浓度为2898 mg/m3. 吸收实验在常压下进行, 通过水浴控温, 实验设定的温度范围为室温到80 ℃. 测定H2S吸收性能的实验装置是由气瓶(H2S和N2)、 质量流量计、 混合器、 吸收装置、 气体分析仪以及尾气处理等部分组成[3], 其中吸收装置采用U型玻璃管(含有鼓泡砂芯使气体均匀分散), 内径为1.0 cm.
1.3 计算方法
在B3LYP/6-31G* 水平上进行几何构型优化, 计算了H2S分子、 IL和MDEA之间结合后放出的热量. 所涉及的量子化学计算由Gaussian 03程序和SGI工作站完成[26].
2 结果与讨论
2.1 功能化离子液体的FTIR表征
图1为合成的3种功能化离子液体的红外光谱图. 从图1(A) [Bmim]HCO3离子液体的谱图可以看出, 3421 cm-1处的吸收峰对应的是缔合— OH伸缩振动, 3149和3092 cm-1处的吸收峰为芳环上的C— H伸缩振动, 2873与2963 cm-1处的吸收峰为脂肪族的C— H伸缩振动, 1638 cm-1处的吸收峰为C=的伸缩振动, 1569 cm-1处的吸收峰为芳环的骨架振动, 1465和1382 cm-1处的吸收峰为甲基对称变形振动和弯曲伸缩振动, 1169 cm-1处的吸收峰为芳环C— H面内弯曲振动, 950 cm-1处的吸收峰为HC O−3O3- 中OH…O 之间的非平面弯曲振动, 表明[Bmim]HCO3具有[BMIM]+和HC O−3O3- 的结构特征[27]. 图1(B)为[TMG]L离子液体的红外光谱. 可以看出, 3500~3000 cm-1属于— OH的伸缩振动峰, 2972 cm-1处对应的是— CH3中的C— H的伸缩振动, 其中CH3— N和N— H的特征峰分别出现在2818和1611 cm-1处[28]. 从图1(C)[MEA]L离子液体的光谱中可以看出, 3500~2800 cm-1间的峰属于胺的典型峰, 3382 cm-1处有— OH伸缩振动峰与N— H伸缩振动峰的结合, 1578 cm-1处有— COO–的反对称伸缩振动峰与N— H弯曲振动峰的结合, 1415 cm-1处有— COO–的对称伸缩振动峰, 1072 cm-1处有C— N的伸缩振动峰, 表明[MEA]L具有乙醇胺和乳酸的结构特征[29].
Fig.1
 |
Fig.1 FTIR spectra of [Bmim]HCO3(A), [TMG]L(B) and [MEA]L(C) |
2.2 功能化离子液体的热重表征
图2所示为功能化离子液体([Bmim]HCO3, [TMG]L和[MEA]L)的TGA-DSC曲线. 从图2中的TG曲线可以看出, 3种离子液体各自出现一个失重台阶, 并且在100 ℃以下其质量损失均小于5.6%, 相应的DSC曲线上出现了不同位置的吸热峰, 其中[MEA]L离子液体的DSC曲线上有2个吸热峰, 分别在202和253 ℃处, 说明该离子液体有2次热分解, 可以确定在实验温度(室温~80 ℃)下3种功能化离子液体的热稳定性良好.
Fig.2
 |
Fig.2 TGA(a) and DSC(b) curves of [Bmim]HCO3(A), [TMG]L(B) and [MEA]L(C) |
2.3 不同离子液体复配脱硫剂对H2S的吸收性能
室温(28 ℃)下, 功能化离子液体([MEA]L, [TMG]L和[Bmim]HCO3)和常规离子液体([Bmim]BF4和[Bmim]Cl)与MDEA水溶液混合得到的新型复配脱硫剂对H2S的吸收性能如图3所示.
Fig.3
 |
Fig.3 H2S absorption efficiency as a function of time on different IL-MDEA-H2O combined desulfurizers |
可以看出, 在MDEA水溶液中添加离子液体的脱硫效果依次为[Bmim]Cl> [Bmim]HCO3> [Bmim]BF4> None> [TMG]L> [MEA]L. 单一MDEA水溶液60 min后的脱硫效率为87%, [Bmim]BF4, [Bmim]Cl和[Bmim]HCO3离子液体复配体系的脱硫效率要优于单一MDEA水溶液, 而添加[MEA]L和[TMG]L离子液体后, 脱硫效率反而下降. 由此可见, 添加常规离子液体后的脱硫效果要优于某些功能化离子液体.
硫容量[S(g· L-1)]的计算公式为
S=32AcQ34V×10−6(1)S=32AcQ34V×10-61
式中, A为Origin软件对各曲线在一定时间段内的积分, c为H2S的初始浓度(mg/m3); Q为H2S气体流量(mL/min); V为吸收剂体积(mL). 计算的结果是从吸收开始到吸收效率降至低于10%时间段内的硫容. 由此得到复配脱硫剂的硫容分别为: MDEA-H2O, 2.19 g/L; [MEA]L-MDEA-H2O, 0.48 g/L; [TMG]L-MDEA-H2O, 1.94 g/L; [Bmim]BF4-MDEA-H2O, 3.06 g/L; [Bmim]HCO3-MDEA-H2O 3.51 g/L; [Bmim]Cl-MDEA-H2O, 3.66 g/L. 可以看出, 在MDEA-H2O中添加[Bmim]BF4, [Bmim]HCO3和[Bmim]Cl离子液体脱硫能力增强, 而添加[MEA]L和[TMG]L离子液体, 脱硫能力反而下降, 说明含有乳酸根的离子液体可能阻碍了醇胺对H2S的吸收.
[Bmim]BF4, [Bmim]HCO3, [TMG]L和[MEA]L离子液体在25 ℃时的黏度分别为233[30], 22[31], 415.4[32], 817.5[33] mPa· s, 而[Bmim]Cl离子液体在25 ℃时为固态, 从实验结果看, 由于投加量较低, 离子液体本身的黏度与复合体系脱硫效率之间并无关联.
2.4 不同温度下复配脱硫剂对H2S的吸收性能
Ma等[34]合成了一系列醇胺类离子液体, 并用于烟气脱硫性能的研究, 结果发现, 随着温度上升, 脱硫效率反而下降. 在本实验中, 针对脱硫性能优异的[Bmim]Cl-MDEA-H2O复配体系, 其在不同温度下的脱硫性能如图4所示. 随着温度的升高, 吸收性能降低. 温度对脱硫性能的影响存在3方面原因: (1) 温度的升高使反应速率增大, 使气体在脱硫剂中的传质更好; (2) 温度的升高会降低气体在脱硫剂中的溶解度; (3) 低温有利于有机胺对H2S的吸收[34].
Fig.4
 |
Fig.4 H2S absorption efficiency by [Bmim]Cl-MDEA-H2O combined deoxidizer as a function of time at 28 ℃(a), 60 ℃(b) and 80 ℃(c) Desulfurizer: 10 mL; [Bmim]Cl: 1 g; MDEA: 3 g. |
2.5 不同配比脱硫剂对H2S的吸收性能
单次吸收使用的复配脱硫剂总量为10 mL, 不同质量离子液体和MDEA的脱硫剂对H2S的吸收效率的影响列于表1. 可以看出, 在未添加离子液体的情况下, 10 mL MDEA水溶液(含MDEA 分别为1, 3和5 g)吸收H2S 60 min后的效率分别为72.5%, 84.8%和89.1%; 在未使用MDEA的情况下, 10 mL H2O、 10 mL [Bmim]Cl水溶液(含1 g IL)和10 mL [Bmim]Cl(80 ℃)吸收H2S 5 min时的效率均非常低, 分别为17.6%, 14.9%和9.8%. 从上述结果可知, 单一MDEA水溶液对H2S的吸收起决定性作用, 纯离子液体虽然比离子液体水溶液以及纯水的脱硫效果差, 但是在保证脱硫剂总体积和MDEA质量不变的情况下, 增加[Bmim]Cl的质量, 脱硫效率显著提高. 因此, 在MDEA水溶液中加入[Bmim]Cl离子液体可以有效提高复配体系的脱硫性能, 其中[Bmim]Cl与体系各组分之间的作用尤为关键.
Table 1
Table 1

Table 1 H2S absorption capacity and sulfur capacity of [Bmim]Cl-MDEA-H2O combined eoxidizer with different component
a. Value was tested at 60th min and the absorption temperature was 28 ℃; b. value was tested at 5th min; c. value was tested within a period time until the absorption efficiency decreased below 10%. |
Table 1 H2S absorption capacity and sulfur capacity of [Bmim]Cl-MDEA-H2O combined eoxidizer with different component |
2.6 离子液体的消泡性能
为了便于研究, 减少脱硫剂用量为5 mL, MDEA和离子液体均添加0.5 g, 测得脱硫剂在吸收器中静止时的高度为6 cm, 在鼓泡吸收H2S的实验过程中, 记录吸收30 min时的脱硫剂(含气泡)高度, 数据列于表2. 可以看出, 除了[TMG]L, 其它离子液体均具有不同程度的消泡作用, 其中[Bmim]HCO3离子液体消泡效率最高(46.4%); 并且随着[Bmim]HCO3在脱硫剂中比例的增加而提高, 在5 mL脱硫剂中添加1.5 g [Bmim]HCO3, 消泡效率提高到64.5%. 可见, 在MDEA水溶液中添加合适的离子液体, 如[Bmim]Cl, [Bmim]BF4或[Bmim]HCO3, 既能够增进H2S的吸收, 又可以大幅度消减MDEA水溶液单独吸收所产生的泡沫, 总体效果显著优于MDEA水溶液.
Table 2
Table 2

Table 2 Capacity of ILs on eliminating bubbles
|
Table 2 Capacity of ILs on eliminating bubbles |
2.7 脱硫机理
H2S与醇胺溶液反应生成铵盐, 铵盐经过加热分解而恢复为醇胺并同时释放出H2S. 复配脱硫剂中离子液体与H2S的作用是物理吸收还是化学吸收或两者兼有与离子液体的种类有关. Pomelli等[26]研究了H2S与[Bmim]+离子液体([Bmim]Cl, [Bmim]BF4, [Bmim]PF6, [Bmim]TfO和[Bmim]Tf2N)的相互作用, 通过对 1H, 13C, 31P, 19F和 11B的核磁检测, 发现这些离子液体并不与H2S反应. 因此, 本文中所用的[Bmim]Cl和[Bmim]BF4离子液体与硫化氢的作用仅为物理吸收. 根据文献[35]报道, 功能化离子液体[TMG]L和[MEA]L对H2S既有物理吸收又有化学吸收; 对于[Bmim]HCO3离子液体, 其阴离子HC O−3O3- 与H2S不反应, 因此也只有物理吸收. 由于实验在常压下进行, 因此相对于化学吸收来说, 物理吸收可以忽略. 结合脱硫效率发现, 只有物理吸收的离子液体复配脱硫剂脱硫效率要高于同时有物理和化学吸收的功能化离子液体复配脱硫剂, 因此, 脱硫效率与离子液体和H2S之间的作用关联不大.
Tang等[36]用密度泛函理论计算的方法研究了CO 在M55(M=Cu, Ag, Au)团簇上的吸附, 并考察了电荷对吸附的影响, 发现金团簇的电荷对吸附能影响较大, 而银和铜团簇的电荷对吸附能影响较小. Pomelli等[26]通过密度泛函方法从分子水平对H2S与离子液体阴离子之间的相互作用进行的研究验证了H2S在离子液体中的溶解度大小. Wang等[37]也用此方法计算并研究了水分子与离子液体的相互作用, 揭示了离子液体和水混合体系的性质. [Bmim]HCO3, [TMG]L, [MEA]L, [Bmim]Cl和[Bmim]BF4的结构式如图5所示. 本文采用密度泛函B3LYP方法, 优化了图5所示的5种离子液体以及MDEA和H2S分子的几何结构, 计算了单个分子的能量、 2种分子复合体的总能量以及分子之间结合释放的热量, 结果列于表3.
Fig.5
 |
Fig.5 Chemical structures of [Bmim]Cl, [Bmim]BF4, [Bmim]HCO3, [TMG]L and [MEA]L |
Table 3
Table 3

Table 3 Energetics data on IL-MDEA , IL-H2S and MDEA-H2S
a. The energy of ionic liquid; b. the total energy of two substances; c. the energy of two substances released after combination; E0 of H2S is -1673.5 kJ/mol. |
Table 3 Energetics data on IL-MDEA , IL-H2S and MDEA-H2S | |||||||||||||||||||||||||||||||||||||||||||||||||||||
从表3可以看出, MDEA与5种离子液体的结合能均为负值, 说明结合过程是放热的, 并且负值越大, 结合能越大, 结合后物质越稳定, 因此, 可以得到离子液体与MDEA混合后的稳定性大小顺序为[Bmim]Cl-MDEA> [Bmim]HCO3-MDEA> [Bmim]BF4-MDEA> [TMG]L-MDEA> [MEA]L-MDEA, 这与H2S的吸收效率的顺序一致. 在吸收H2S的反应中, H2S分子与复配脱硫剂中各组分(离子液体、 MDEA和H2O)的结合能也在表3中列出, 其中H2S与[MEA]L离子液体的结合能为正值, 表明该反应吸热; 与其它组分的结合能均为负值, 同样可得到H2S与各组分混合后稳定性大小顺序为[Bmim]HCO3-H2S> [Bmim]Cl-H2S> [TMG]L-H2S> [Bmim]BF4-H2S> H2O-H2S> MDEA-H2S> [MEA]L-H2S. 理论上添加[Bmim]HCO3, [Bmim]Cl, [TMG]L和[Bmim]BF4这4种离子液体, 由于其与H2S作用强烈, 结合稳定, 更能够促进与MDEA复配后的脱硫, 但其中[TMG]L-MDEA-H2O复配脱硫剂比MDEA-H2O脱硫效果要差, 同样含有乳酸根的[MEA]L-MDEA-H2O脱硫剂也表现出较低的脱硫效率, 这可归因于[TMG]L和[MEA]L离子液体与MDEA结合能数值均较小, 体系本身稳定性变差, 阻碍了MDEA对H2S的吸收. 因此, 对于脱硫效率而言, 离子液体和MDEA结合稳定性是主要贡献因素.
2.8 复配脱硫剂的再生
采用10 mL脱硫剂(其中含有1 g [Bmim]Cl和1 g MDEA) 吸收H2S直至基本饱和, 所用时间为270 min, 在60 ℃下, 通入300 mL/min的空气进行再生, 并监测空气中的H2S浓度, 测试180 min. 为了确定复配吸收剂是否得到完全再生, 通入臭氧30 min对再生后的吸收剂进行深度氧化, 在水存在的情况下, 不稳定的— HS键理论上被氧化成S O2−4O42- , 采用离子色谱仪对再生液进行离子浓度测试, 结果列于表4. 可见脱硫剂再生效率[Bmim]BF4-MDEA-H2O> [Bmim]HCO3-MDEA-H2O> [Bmim]Cl-MDEA-H2O, 但相差不大, H2S与离子液体结合能越大, 越不易被空气再生, 使再生程度降低, 但是结合能越大越有利于吸收. 3种高效脱硫剂的再生效率均高于94%.
Table 4
Table 4

Table 4 Regeneration analysis data of desulfurizer
a. The concentration tested by ion chromatograph in dilute solution of 100 mL; b. the quality of sulfur per liter desulfurizer after regeneration; c. value was caculated according to residue sulfur and sulfur capacity. |
Table 4 Regeneration analysis data of desulfurizer |
3 结 论
低温有利于复配脱硫剂对H2S的吸收; 在室温下, 相同质量配比的复配脱硫剂脱硫效果为[Bmim]Cl-MDEA-H2O> [Bmim]HCO3-MDEA-H2O> [Bmim]BF4-MDEA-H2O> MDEA-H2O> [TMG]L-MDEA-H2O> [MEA]L-MDEA-H2O. 单一MDEA水溶液60 min后的脱硫效率为87%, 添加[Bmim]Cl, [Bmim]HCO3和[Bmim]BF4离子液体后, 脱硫效率可高达97%, 明显优于单一MDEA水溶液; 除了[TMG]L, 其它离子液体均具有不同程度的消泡作用, 其中[Bmim]HCO3离子液体消泡效率最高, 为46.4%, 并且随着[Bmim]HCO3在脱硫剂中比例的增加而升高. 通过密度泛函理论计算, 在H2S的吸收效率方面, 离子液体和MDEA结合的稳定性为主要贡献因素. 复配脱硫剂[Bmim]BF4-MDEA-H2O, [Bmim]HCO3-MDEA-H2O和[Bmim]Cl-MDEA-H2O通入空气可基本再生, 并且再生效率分别为94.89%, 94.74%和94.66%.
The authors have declared that no competing interests exist.
参考文献
| [1] | Zhu G. Y. , Dai J. X. , Zhang S. C. , Li J. , Shi D. , Wen Z. G. , Nat. Gas Geoscience, 2004, 15(2), 166—170 (朱光有, 戴金星, 张水昌, 李剑, 史斗, 文志刚. 天然气地球科学, 2004, 15(2), 166—170) [本文引用:1] |
| [2] | Schmid R. , Cross J. B. , Latimer E. G. , Energy Fuels, 2009, 23, 3612—3616 [本文引用:1] |
| [3] | Ma Y. Q. , Yang F. , Wang R. , Chin. J. Inorg. Chem. , 2012, 28(10), 2179—2185 (马云倩, 杨烽, 王睿. 无机化学学报, 2012, 28(10), 2179—2185) [本文引用:2] |
| [4] | Cadours R. , Roquet D. , Perdu G. , Ind. Eng. Chem. Res. , 2007, 46(1), 233—241 [本文引用:1] |
| [5] | Zhang J. J. , Song H. , Bai B. , Wang L. , Ind. Eng. Prog. , 2012, 31(7), 1432—1436 (张静娇, 宋华, 白冰, 王璐. 化工进展, 2012, 31(7), 1432—1436) [本文引用:1] |
| [6] | Huttenhuis P. J. G. , Agrawal N. J. , Hogendoorn J. A. , Versteeg G. F. , J. Pet. Sci. & Eng. , 2007, 55(1/2), 122—134 [本文引用:1] |
| [7] | Li C. , Furst W. , Chem. Eng. Sci. , 2000, 55(15), 2975—2988 [本文引用:1] |
| [8] | Qian Z. , Xu L. B. , Li Z. H. , Li H. , Guo K. , Ind. Eng. Chem. Res. , 2010, 49(13), 6196—6203 [本文引用:1] |
| [9] | Mazloumi S. H. , Haghtalab A. , Jalili A. H. , Shokouhi M. , J. Chem. Eng. Data, 2012, 57(10), 2625—2631 [本文引用:1] |
| [10] | Fouad W. A. , Berrouk A. S. , Ind. Eng. Chem. Res. , 2012, 51(18), 6591—6597 [本文引用:1] |
| [11] | Sakhaeinia H. , Jalili A. H. , Taghikhani V. , Safekordi A. A. , J. Chem. Eng. Data, 2010, 55(12), 5839—5845 [本文引用:1] |
| [12] | Jou F. Y. , Mather A. E. , Int. J. Thermophys. , 2007, 28, 490—495 [本文引用:1] |
| [13] | Sakhaeinia H. , Taghikhani V. , Jalili A. H. , Mehdizadeh A. , Safekordi A. A. , Fluid Phase Equilib. , 2010, 298(2), 303—309 [本文引用:1] |
| [14] | Ghobadi A. F. , Taghikhani V. , Elliott J. R. , J. Phys. Chem. B, 2011, 115(46), 13599—13607 [本文引用:1] |
| [15] | Tokuda H. , Hayamizu K. , Ishii K. , Susan M. A. B. H. , Watanabe M. , J. Phys. Chem. B, 2004, 108(42), 16593—16600 [本文引用:1] |
| [16] | Shang Y. , Li H. , Zhang S. , Xu H. , Wang Z. , Zhang L. , Zhang J. , J. Chem. Eng. , 2011, 175, 324—329 [本文引用:1] |
| [17] | Huang J. , Riisager A. , Berg R. W. , Fehrmann R. , J. Mol. Catal. A: Chem. , 2008, 279(2), 170—176 [本文引用:1] |
| [18] | Gutowski K. E. , Maginn E. J. , J. Am. Chem. Soc. , 2008, 130(44), 14690—14704 [本文引用:1] |
| [19] | Guo L. Y. , Shi T. J. , Li Z. , Duan Y. P. , Wang Y. G. , Chem. J. Chinese Universities, 2008, 29(9), 1901—1907 (郭立颖, 史铁钧, 李忠, 段衍鹏, 王于刚. 高等学校化学学报, 2008, 29(9), 1901—1907) [本文引用:1] |
| [20] | Liang D. , Xin X. , Duan H. , Yin Y. , Gao H. , Lin Y. , Xu J. , Chem. Res. Chinese Universities, 2008, 24(1), 36—41 [本文引用:1] |
| [21] | Guo B. , Duan E. , Zhong Y. , Gao L. , Zhang X. , Zhao D. , Energy Fuels, 2011, 25, 159—161 [本文引用:1] |
| [22] | Heintz Y. J. , Sehabiague L. , Morsi B. I. , Jones K. L. , Luebke D. R. , Pennline H. W. , Energy Fuels, 2009, 23(10), 4822—4830 [本文引用:1] |
| [23] | Duan E. , Guo B. , Zhang M. , Guan Y. , Sun H. , Han J. , J. Hazard. Mater. , 2011, 194, 48—52 [本文引用:1] |
| [24] | Yusoff R. , Aroua M. K. , Shamiri A. , Ahmady A. , Jusoh N. S. , Asmuni N. F. , Bong L. C. , Thee S. H. , J. Chem. Eng. Data, 2013, 58(2), 240—247 [本文引用:1] |
| [25] | Wang Z. L. , Xu F. , Xing X. L. , Ren Z. B. , Chem. Ind. & Eng. Prog. , 2013, 32(2), 394—399 (王占丽, 徐凡, 邢小林, 任增保. 化工进展, 2013, 32(2), 394—399) [本文引用:1] |
| [26] | Pomelli C. S. , Chiappe C. , Vidis A. , Laurenczy G. , Dyson P. D. , J. Phys. Chem. B, 2007, 111(45), 13014—13019 [本文引用:3] |
| [27] | Yue Q. F. , Wang C. X. , Zhang L. N. , Ni Y. , Jin Y. X. , Polymer Degradation and Stability, 2011, 96(4), 399—403 [本文引用:1] |
| [28] | Wu W. , Han B. , Gao H. , Liu Z. , Jiang T. , Huang J. , Angew. Chem. Int . Ed. , 2004, 43(18), 2415—2417 [本文引用:1] |
| [29] | Ji J. R. , Yuan H. T. , Wang J. Y. , Fu L. L. , Du Z. L. , Hu Y. Q. , Hebei Journal of Industrial Science and Technology, 2010, 27(5) 285—287(纪俊荣, 袁海涛, 王建英, 付林林, 杜振雷, 胡永琪. 河北工业科技, 2010, 27(5), 285—287) [本文引用:1] |
| [30] | Li R. X. , Green Solvent-nthesis and Application of Ionic Liquid, Chemical Industry Press, Beijing, 2004, 20—25 (李汝雄. 绿色溶剂-子液体的合成与应用, 北京: 化学工业出版社, 2004, 20—25) [本文引用:1] |
| [31] | Wang X. D. , Wu W. Y. , Tu G. F. , Jiang K. X. , Chin. Sci. Bull. , 2009, 54(1), 21—26)(王晓丹, 吴文远, 涂赣峰, 蒋开喜. 科学通报, , 2009, 54(1), 21—26) [本文引用:1] |
| [32] | Yu G. , Zhang S. , Fluid Phase Equilib. , 2007, 255, 86—92 [本文引用:1] |
| [33] | Zhai L. Z. , Zhong Q. , Du H. C. , He C. , Wang J. , Journal of Chemical Industry and Engineering, 2009, 60(2), 450—454(翟林智, 钟秦, 杜红彩, 何川, 王娟. , 2009, 60(2), 450—454) [本文引用:1] |
| [34] | Ma X. L. , Wang X. X. , Song C. S. , J. Am. Chem. Soc. , 2009, 131(16), 5777—5783 [本文引用:2] |
| [35] | Jin M. , Hou Y. , Wu W. , Ren S. , Tian S. , Xiao L. , Lei Z. , J. Phys. Chem. B, 2011, 115(20), 6585—6591 [本文引用:1] |
| [36] | Tang D. Y. , Hu J. P. , Lü S. Z. , Sun G. F. , Zhang Y. Q. , Acta Chim. Sinica, 2012, 70(8), 943—948(唐典勇, 胡建平, 吕申壮, 孙国峰, 张元勤. 化学学报, 2012, 70(8), 943—948) [本文引用:1] |
| [37] | Wang Y. , Li H. , Han S. , J. Phys. Chem. B, 2006, 110(48), 24646—24651 (Ed. : V, Z) [本文引用:1] |
 微信
微信
 支付宝
支付宝