离子液体的超级电容器和电池应用
表1一些电化学适用离子液体的性质1
| 离子液体 | 熔点 (°C) | 粘度 (mm/s 25 °C) | 电导率 (mS/cm) | 电化学 窗口(V) |
| 1-乙基-3-甲基咪唑啉双(三氟甲基磺酰基)亚胺(EMI-TFSI) | -17 | 18 | 8.8 | 4.1 |
| 1-乙基-3-甲基咪唑三氟甲磺酸盐(EMI-OTf) | -9 | 43 | 9.2 | 4.1 |
| 1-丁基-1-甲基吡咯烷双(三氟甲磺酰)亚胺(BMP-TFSI) | -50 | 71 | 2.2 | 5.5 |
| 1-己基-3-甲基咪唑六氟磷酸盐(HMI-PF6) | -80 | 548 | 1 | 5.5 |
| 1-乙基-3-甲基咪唑二氨腈(EMI-DCA) | -21 | 17 | 27 | 5.9 |
| 1-甲基-3-辛基咪唑四氟硼酸盐-(MOI-BF4) | -88 | 422 | 0.43 | 6 |
电化学电容器(超级电容器)
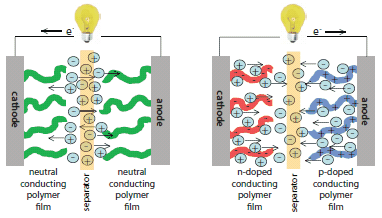
电化学电容器(EC),又称作超级电容器,是功率平衡的电荷储存装置,使用电活性聚合物的氧化还原、金属氧化物或碳质材料储存电能。充电过程中,EC电极被还原(阴极)和被氧化(阳极)来储存电能,之后在放电过程中电能被释放,电极材料则回到中性状态。图3解释了IV型EC的一般运行,结合p型掺杂(阳极)和n型掺杂(阴极)聚合物以达到最高储能。

图3. 以电活性聚合物为基础的电化学容器原理图显示充电(左)和放电(右)期间的电子流动和离子运动。充电期间,阴极(n掺杂)聚合物带负电,电解液中阳离子进入电极补偿电荷。同时,阳极(p掺杂)聚合物带正电,电解液中阴离子进入电极补偿电荷。放电期间,两极聚合物都回到中性状态,离子也回到溶液。
EC最重要的应用包括便携式电子产品的内存保护系统、电力设施的负荷平衡和电动汽车储能。EC通常比电池提供更多的单位质量功率并且比传统电容器储存更多的单位质量能量。因此,它们可用于提供电动汽车的突发功率。所有EC都需要电解液才能运行;使用离子液体7,12后可以弃用挥发性有害溶剂并提高这些装置的运行稳定性。
锂离子电池
锂离子电池在电子消费市场到处可见,最终可能主导商用大型高功率储能。锂电池由电解液分隔的嵌锂氧化物和碳两种电极组成(图4)。随着电池充电,锂离子从氧化电极移动到碳电极,储存电能。当电池放电时,锂离子回到氧化电极,于是电能被释放。锂离子传输由电解液协助,它通常含有易挥发易燃溶剂。因此,安全性是含有传统电解液的锂电池的主要考虑事项。易燃溶剂存在下,短路或局部过热会导致热失控、起火甚至爆炸。离子液体替代易燃溶剂提高了电池安全性,对锂离子电池特别有用。10

图4. 锂离子电池在放电(左)和充电(右)期间的电子流动和锂离子运动。
此外,与电化学电容器电解液不同,离子电池电解液必须协助锂离子传输、在高负电位下保持稳定和支持电池的稳定运行。离子液体满足这些要求是可能的,有好几个研究团队正在研究这个领域。10,13试验过的离子液体包括N-丁基-N-乙基吡咯烷双(三氟甲基磺酰基亚胺);乙基甲基咪唑啉双(三氟甲基磺酰基亚胺);N-甲基-N-丙基吡咯烷双(三氟甲基磺酰基亚胺)和N-甲基-N-丙基哌啶双(三氟甲基磺酰基亚胺)。以上任何一种都可用于制备双(三氟甲烷)磺酰亚胺锂盐溶液,其中锂离子是活性材料。
极端温度下的离子液体
随着对能源生产和储存的日益关注,对广泛温度下运行的电荷储存装置的需求也在增长。在汽车行业,电荷储存装置理想情况下可在低至-30°C的温度下运行。14电荷储存装置的军用要求甚至更严格,某些应用的目标温度低至-60°C。15大多数电池在较低温度下遭遇性能严重下降,尤其是-60°C以下。16除了减慢充电/放电过程的动力学之外,较低温度也会增加电解液粘度,降低电解液输送电荷的能力。这样的性质变化导致装置性能下降或长时间暴露于低温时故障。低温对溶液电解液最严重的影响之一是降低电解液材料的溶解度,导致盐沉淀和电化学电容器或电池的损坏。根据表1的证据显示,许多离子液体电解液能在汽车行业要求的适度低温下运行,但很少能在军用所需的极低温度下运作。17更挑战的是这些电解液要在同样的宽温度区间支持各种单体/聚合物体系的电化学过程(沉积、氧化、还原、装置运行15等)。不幸的是,只有少数ILE在极低温度下保持液态,而它们的粘度对大多数电化学应用而言会变得过高。混合不同离子液体或使用降粘剂可以帮助缓解这个问题。电化学装置在高达60°C的高温下的性能也是能量储存工业中的关注点。14不幸的是,大多数溶剂型电解液在高温下会遭遇溶剂高挥发性。溶剂蒸发在密封系统中会导致起火和爆炸;而在开放系统中,它会导致电解液沉淀、电荷储存材料损坏以及电荷储存能力损失。因此,离子液体极低的挥发性使其成为用于高温的电解液的优异选择。
纯度要求
储能应用中电解液的纯度对于电化学装置的稳定性和性能十分重要。离子液体也不例外。根据离子液体制备所用的合成路线,材料中的杂质可能包括水、多余阳离子或阴离子、或其他溶剂。就算痕量污染物也会导致不良副反应并影响EAP型装置的性能。因此,氯化物和水杂质已证明会影响离子液体的粘度。21, 22微量(几ppm)溶剂例如氧化铝和二氧化硅也会导致电化学性能损失。23生产适合电化学使用的离子液体的纯化方法通常涉及柱层析或真空蒸馏(以去除挥发杂质;离子液体本身不会蒸发)。许多使用常用材料的方法已经发表,应该认真遵守。21-23
参考文献
- Galínski, M.; Lewandowski, A.; Stepniak, I. Electrochim. Acta 2006, 51, 5567.
- Pringle, J. M.; MacFarlane, D. R.; Forsyth, M. Synth. Met. 2005, 155, 684.
- Gottesfeld, S.; Ferraris, J. P.; Rudge, A.; Raistrick, I. Electrochim. Acta 1994, 39, 273.
- Novák, P.; Müller, K.; Santhanam, K. S. V.; Haas, O. Chem. Rev. 1997, 97, 207.
- Monk, P. M. S.; Mortimer, R. J.; Rosseinsky, D. R. Electrochromism:Fundamentals and Applications, VCH, Weinheim, 1995.
- Irvin, J. A.; Irvin, D. J.; Stenger-Smith, J. D. Electrically Active Polymers for Use in Batteries and Supercapacitors. in Handbook of Conducting Polymers, 3rd ed.; Skotheim, T., Ed.; Reynolds, J. R., Ed.; Taylor & Francis, Boca Raton, FL, 2008.
- Stenger-Smith, J. D.; Webber, C. K.; Anderson, N. A.; Chafin, A. P.; Zong, K.; Reynolds, J. R. J. Electrochem. Soc. 2002, 149, A973.
- Pringle, J. M. Polymer 2005, 46, 2047.
- Zakeeruddin, S. M.; Graetzel, M. Adv. Funct. Mater. 2009, 19(14), 2187.
- Armand, M.; Endres, F.; MacFarlane, D. R.; Ohno, H.; Scrosati, B. Nature Mater. 2009, 8, 621.
- Irvin, D. J.; Stenger-Smith, J. D.; Irvin, J. A. Electrochemical Supercapacitors Based on Poly(Xylyl Viologen) Polymer Preprints 2007, 48, 150.
- Balducci, A.; Henderson, W. A.; Mastragostino, M.; Passerini, S.; Simon, P.; Soavi, F. Electrochim. Acta 2005, 50, 2233.
- Matsumoto, H.; Sakebe, H.; Tatsumi, K. J. Power Sources, 2006, 160, 1308.
- Pesaran, A. A.; Markel, T.; Tataria, H. S.; Howell, D. “Battery Requirements for Plug-In Hybrid Electric Vehicles – Analysis and Rationale,” Conference Paper July 2009 NREL/ CP-540-42240.
- Department of Defense Test Method Standard MIL-STD-810G Method 502.5 (Low Temperature). http://www.dtc.army.mil/publications/MIL-STD-810G.pdf (accessed October 2009)
- Arbizzani, C.; Mastragostino, M.; Scrosati, B. in Handbook of Conducting Polymers, 2nd ed.; Skotheim, T. A., Ed.; Elsenbaumer, R. L., Ed.; Reynolds, J. R., Ed.; Marcel Dekker, NY 1998.
- Aurbach, D. Electrochim. Acta 2004, 50, 247.
- Endres, F. Electrodeposition from Ionic Liquids, Abbott, A., Ed.; MacFarlane, D. R., Ed.; Wiley-VCH, Weinheim, Germany, 2008.
- Greaves, T. L.; Drummond, C. J. Chem. Rev. 2008, 108, 206.
- Ding, J.; Zhou, D.; Spinks, G.; Wallace, G.; Forsyth, S.; Forsyth, M.; MacFarlane, D. Chem. Mater. 2003, 15, 2392.
- Seddon, K. R.; Stark, A.; Torres, M. J. Pure Appl. Chem. 2000, 72, 2275.
- Zhang, J.; Bond, A. M. The Analyst 2005, 130, 1132.
- Clare, B. R.; Bayley, P. M.; Best, A. S.; Forsyth, M.; MacFarlane, D. R. Chem. Commun. 2008, 2689.
微信
支付宝